1前言
多數(shù)礦樣中都含有氯離子���,氯離子的存在對(duì)鈍態(tài)金屬(比如不銹鋼)起到直接的破壞作用;原因是氯離子與鈍態(tài)金屬會(huì)發(fā)生應(yīng)力腐蝕����,處于鈍態(tài)的金屬仍有一定的反應(yīng)能力���,即鈍化膜的溶解和修復(fù)(再鈍化)處于動(dòng)平衡狀態(tài)��。當(dāng)介質(zhì)中含有氯離子時(shí)��,平衡便受到破壞�����,溶解占優(yōu)勢(shì)�����。其原因是氯離子能優(yōu)先地有選擇性的吸附在鈍化膜上�,把氧原子排擠掉���,然后和鈍化膜中的陽(yáng)離子結(jié)合成可溶性氯化物�����,結(jié)果在新露出的基底金屬的特定點(diǎn)上生成小蝕坑(孔徑多在20~30μm)���,這些小蝕坑稱為孔蝕核��,孔蝕一旦形成則加速生長(zhǎng)����,從而大面積的腐蝕金屬設(shè)備�,降低設(shè)備的使用壽命;因此每個(gè)企業(yè)對(duì)礦樣中氯離子含量的指標(biāo)都有嚴(yán)格要求,能夠準(zhǔn)確���、快速測(cè)量出氯離子含量尤為重要���。
目前測(cè)定氯離子的方法有硝酸銀滴定法���、電位滴定法�、離子選擇性電極法��、比色法、汞量滴定法等�。這些方法各有利弊,在生產(chǎn)中應(yīng)用有一定難度�����。分光光度法以其靈敏度高�,選擇性好,操作簡(jiǎn)單等優(yōu)點(diǎn)被廣泛應(yīng)用于化工行業(yè)��。由于氯化銀混濁液不穩(wěn)定�����,直接應(yīng)用分光光度法測(cè)定結(jié)果不理想����。本文通過(guò)研究氯化銀混濁液在明膠-乙醇水溶液中的穩(wěn)定性,建立了一種新的分光光度法��,能夠快速準(zhǔn)確分析出礦石中氯離子的含量���,結(jié)果令人滿意���。
2實(shí)驗(yàn)部分
2.1實(shí)驗(yàn)儀器
2.2實(shí)驗(yàn)試劑
除非另有說(shuō)明����,在實(shí)驗(yàn)中使用的試劑均為分析純�,用水均為蒸餾水。試劑配制如下:
1)氫氧化鈉溶液(200g/L);
2)硝酸(1+1);
3)硝酸(1+10);
4)硝酸銀溶液(2g/L);
5)氯標(biāo)準(zhǔn)溶液(100ug/mL);
稱取0.8243g氯化鈉(優(yōu)級(jí)純�,經(jīng)500~600℃灼燒后冷卻),加水全部溶解后���,移入500mL容量瓶中���,以水定容,搖勻����。此溶液含氯離子1mg/mL。吸取25mL此氯標(biāo)準(zhǔn)溶液于250mL容量瓶中��,以水定容���,搖勻��。此溶液含氯離子100ug/mL��。
6)明膠-乙醇溶液(2+3);
稱取0.1g明膠���,加入100mL熱水溶解,吸取20mL明膠溶液于100mL容量瓶中��,加入30mL乙醇����,以水定容,搖勻����。
作者簡(jiǎn)介:竇輝(1981-),江西貴溪人��,主要從事化驗(yàn)技術(shù)管理工作�。E-mail:dou.hui@163.com
2.3實(shí)驗(yàn)方法
稱取0.1000~0.5000g試樣于300mL燒杯中,加入10mL硝酸(1+10)�,并用玻璃棒不斷攪拌5分鐘,移入到100mL容量瓶中����,加入5mL~10mL200g/L氫氧化鈉溶液,用水定容����。干過(guò)濾���,取10.0mL分液于100mL容量瓶中,用硝酸(1+1)���、氫氧化鈉(200g/L)調(diào)至中性(用PH試紙檢驗(yàn))����,加入2mL明膠-乙醇溶液��,5mL硝酸(1+1)溶液���、2mL硝酸銀(2g/L)溶液�����,用水定容��。靜置15分鐘�����,用1cm吸收池���,在330nm波長(zhǎng)處測(cè)定其吸光度��,與分析試樣同時(shí)做空白試驗(yàn)。從工作曲線上查出相應(yīng)的氯離子的濃度�����。
工作曲線的繪制:分別移取0.00mL�、1.00mL、2.00mL����、3.00mL 、4.00mL�、5.00mL氯標(biāo)準(zhǔn)溶液(100ug/mL)于100mL容量瓶中,用水稀釋至10mL~20mL��,加入2mL明膠-乙醇溶液���、5mL硝酸(1+1)�����、2mL硝酸銀溶液(2g/L)�,用水定容,搖勻�。靜置15分鐘,用1cm吸收池�,以試劑空白為參比在330nm波長(zhǎng)處測(cè)定其吸光度,以氯離子的濃度為橫坐標(biāo)�����,吸光度為縱坐標(biāo)����,繪制工作曲線。
3結(jié)果與討論
3.1最佳波長(zhǎng)的選擇
按實(shí)驗(yàn)方法�����,移取5.00mL氯標(biāo)準(zhǔn)溶液于100mL容量瓶中��,用水吹洗至10mL~20mL�,加入2mL明膠-乙醇溶液、5mL硝酸(1+1)�、2mL硝酸銀溶液(2g/L),用水定容�,搖勻。另取一容量瓶平行做試劑空白��,僅不加氯標(biāo)準(zhǔn)溶液,其余相同�。靜置15分鐘,用1cm吸收池���,以試劑空白為參比�,在280nm~400nm�,每隔10nm測(cè)量一次吸光度���,在吸收峰值附近每隔5nm測(cè)量一次吸光度�����。繪制吸收光譜如圖1:
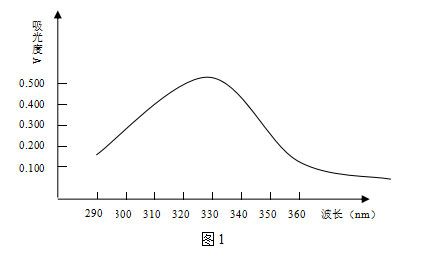
由圖1可見(jiàn)��,該方法的最大吸收波長(zhǎng)為330nm����,因此選擇330nm為測(cè)定波長(zhǎng)�。
3.2硝酸用量的選擇
取9個(gè)100mL容量瓶,按實(shí)驗(yàn)方法���,分別移取5.00mL氯標(biāo)準(zhǔn)溶液于100mL容量瓶中����,用水吹洗至10mL~20mL,加入2mL明膠-乙醇溶液��,分別加入1mL��、2mL��、3mL�、4mL、5mL�、6mL、7mL�、8mL、9mL硝酸(1+1)混勻后����,再加入2mL硝酸銀溶液(2g/L),用水定容����、搖勻;然后靜置15分鐘,以相同的試劑空白為參比測(cè)定其吸光度�����,以吸光度A對(duì)硝酸加入量作圖,如圖2:
實(shí)驗(yàn)表明���,當(dāng)硝酸用量為5mL~7mL時(shí)���,吸光度最大且穩(wěn)定,大于7.5mL時(shí)��,吸光度開(kāi)始下降����。因此該方法硝酸用量采用5mL���。
3.3硝酸銀加入量的選擇
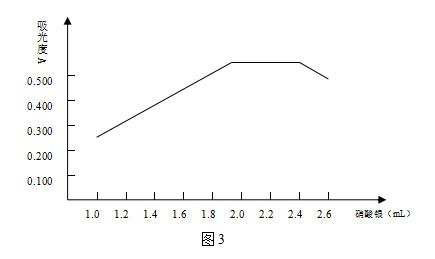
取9個(gè)100mL容量瓶����,按實(shí)驗(yàn)方法��,分別移取5.00mL氯標(biāo)準(zhǔn)溶液于100mL容量瓶中��,用水吹洗至10mL~20mL���,加入2mL明膠-乙醇溶液���,5mL硝酸溶液(1+1)��,混勻后再分別加入1mL���、1.2mL、1.4mL���、1.6mL�、1.8mL�����、2mL�、2.2mL、2.4mL�、2.6mL硝酸銀溶液,用水定容�、搖勻;然后靜置15分鐘,以相同的試劑空白為參比測(cè)定其吸光度�����,以吸光度A對(duì)硝酸銀加入量作圖�����,如圖3:
實(shí)驗(yàn)表明,當(dāng)硝酸銀用量為2mL~2.4mL時(shí)���,吸光度達(dá)到峰值且穩(wěn)定�����,當(dāng)大于2.4mL時(shí)�,吸光度開(kāi)始下降�����,因此該方法顯色劑用量采用2mL�����。
3.4 明膠-乙醇溶液加入量的選擇
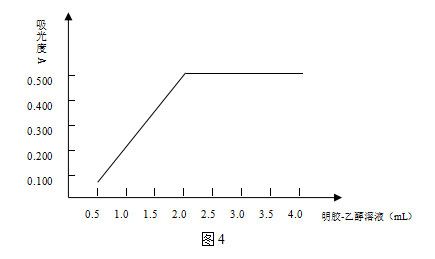
取8個(gè)100mL容量瓶����,按實(shí)驗(yàn)方法�,分別移取5.00mL氯標(biāo)準(zhǔn)溶液于100mL容量瓶中,用水吹洗至10mL~20mL��,分別加入0.5mL、1.0mL���、1.5mL���、2.0mL、2.5mL��、3.0mL��、3.5mL����、4.0mL明膠-乙醇溶液,5mL硝酸(1+1)��,混勻后�,再加入2mL硝酸銀溶液,用水定容��、搖勻����。然后靜置15分鐘,以相同的試劑空白為參比測(cè)定其吸光度�,以吸光度A對(duì)明膠-乙醇溶液加入量作圖�,如圖4:
實(shí)驗(yàn)表明�,當(dāng)明膠-乙醇用量大于2mL時(shí),吸光度最大且穩(wěn)定不變�����,故本方法選擇明膠-乙醇量為2mL���。
3.5溶液穩(wěn)定性試驗(yàn)
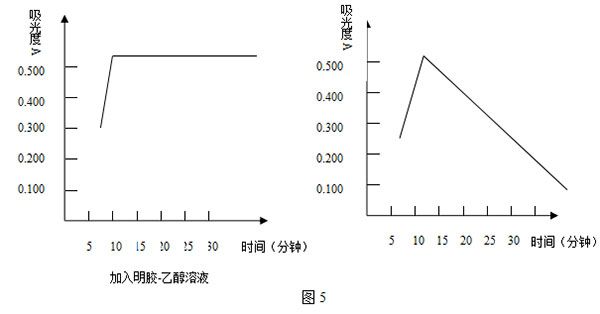
取2個(gè)100mL容量瓶���,按實(shí)驗(yàn)方法,分別移取5.00mL氯標(biāo)準(zhǔn)溶液于100mL容量瓶中��,用水吹洗至10mL~20mL���,第一個(gè)容量瓶加入2mL明膠-乙醇溶液���,5mL硝酸(1+1)����,混勻后,再加入2mL硝酸銀(2g/L)溶液����,第二個(gè)容量瓶不加明膠-乙醇溶液���,其它均相同,用水定容��、搖勻;在不同時(shí)間��,測(cè)定溶液的吸光度����,其結(jié)果如圖5:
明膠屬于水溶性大分子化合物,由于分子結(jié)構(gòu)以及在水溶液中形態(tài)的特點(diǎn)�,可用作光度分析體系的增穩(wěn)、增敏劑�。實(shí)驗(yàn)表明,當(dāng)溶液體系中不加明膠-乙醇溶液時(shí)�����,氯化銀沉淀在該體系中沉淀速度快��,不穩(wěn)定����,隨著時(shí)間延長(zhǎng)吸光度降低���,無(wú)法實(shí)現(xiàn)分光光度法測(cè)定其氯離子的濃度;而加入明膠-乙醇溶液后,體系的穩(wěn)定性增大�����,在穩(wěn)定10分鐘之后可以進(jìn)行測(cè)定���,可以實(shí)現(xiàn)分光光度法測(cè)定氯離子濃度���。
3.6工作曲線范圍
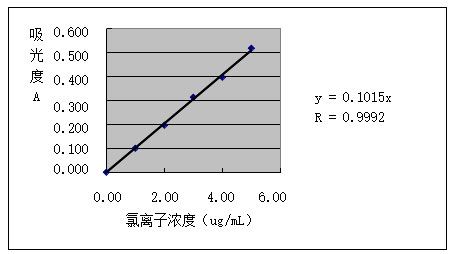
由圖6可以看出,在實(shí)驗(yàn)最佳條件下�,氯離子濃度在0~5ug/mL范圍內(nèi)符合比爾定律,線性回歸方程為y=0.1015x,相關(guān)系數(shù)r=0.9992��,說(shuō)明該方法線性關(guān)系良好��,可作為定量分析的依據(jù)�����。
3.7加標(biāo)回收實(shí)驗(yàn)
按照實(shí)驗(yàn)方法對(duì)樣品加入氯標(biāo)準(zhǔn)進(jìn)行回收實(shí)驗(yàn)并且與另一種方法進(jìn)行對(duì)照確定方法的準(zhǔn)確性��,結(jié)果見(jiàn)表1����、表2。
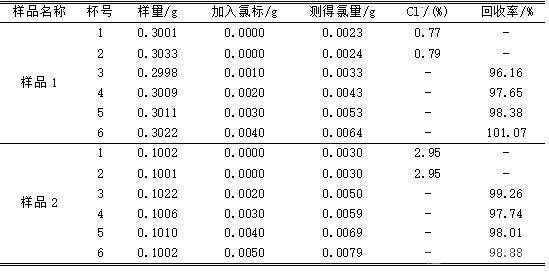
表1 加標(biāo)回收實(shí)驗(yàn)結(jié)果
表2不同方法結(jié)果對(duì)照
表1�����、表2表明�,用本文方法測(cè)定礦石樣品中的氯離子含量,回收率在96.16%~101.07%之間�����,選取的5個(gè)樣品與電位滴定法測(cè)定結(jié)果對(duì)照吻合���,本方法具有較好的準(zhǔn)確度�����。
3.8精密度實(shí)驗(yàn)
稱取7杯樣品3����、樣品4按照實(shí)驗(yàn)方法測(cè)定氯離子含量���,測(cè)定數(shù)據(jù)見(jiàn)表3�。
表3精密度實(shí)驗(yàn)數(shù)據(jù)
表3結(jié)果表明:該方法測(cè)定礦石樣品中的氯離子含量具有較好的精密度。
4結(jié)論
綜上所述��,本方法具有靈敏度高�、準(zhǔn)確度和精密度較好,分析速度快等優(yōu)點(diǎn)�,可用于礦樣中氯離子含量的測(cè)定,具有推廣價(jià)值�。
參考文獻(xiàn):
[1]符斌,李華昌.有色冶金分析手冊(cè).冶金工業(yè)出版社�����,2008
[2]劉珍,黃沛成等.化驗(yàn)員讀本.化學(xué)工業(yè)出版社�����,2010
聲明:
“分光光度法測(cè)定礦樣中氯離子” 該技術(shù)專利(論文)所有權(quán)利歸屬于技術(shù)(論文)所有人���。僅供學(xué)習(xí)研究���,如用于商業(yè)用途,請(qǐng)聯(lián)系該技術(shù)所有人�。
我是此專利(論文)的發(fā)明人(作者)

 1431
編輯:中冶有色技術(shù)網(wǎng)
來(lái)源:江西銅業(yè)集團(tuán)公司貴溪冶煉廠
1431
編輯:中冶有色技術(shù)網(wǎng)
來(lái)源:江西銅業(yè)集團(tuán)公司貴溪冶煉廠




 分享 0
分享 0
 舉報(bào) 0
舉報(bào) 0
 收藏 0
收藏 0
 反對(duì) 0
反對(duì) 0
 點(diǎn)贊 0
點(diǎn)贊 0

 中冶有色技術(shù)平臺(tái)
中冶有色技術(shù)平臺(tái) 2025年03月21日 ~ 23日
2025年03月21日 ~ 23日  2025年03月25日 ~ 27日
2025年03月25日 ~ 27日  2025年03月28日 ~ 30日
2025年03月28日 ~ 30日  2025年03月29日 ~ 31日
2025年03月29日 ~ 31日  2025年04月27日 ~ 29日
2025年04月27日 ~ 29日 
